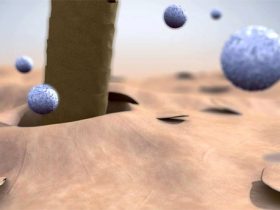
Se denomina micela al conjunto de moléculas que constituye una de las fases de los coloides. Es el mecanismo por el cual el jabón solubiliza las moléculas insolubles en agua, como las grasas. En cosmética, este sistema de acumulación de moléculas entre líquidos coloides se utiliza sobre todo para elaborar productos de limpieza facial. Definición química de la micela
Se denomina micela al conjunto de moléculas que constituye una de las fases de los coloides. Es el mecanismo por el cual el jabón solubiliza las moléculas insolubles en agua, como las grasas.
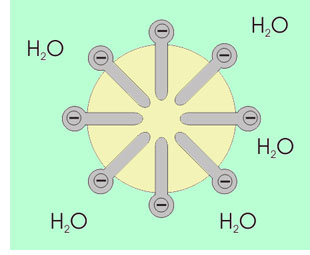 En la formación de una micela de jabón en agua, las moléculas de jabón (una sal de sodio o potasio de un ácido graso) se enlazan entre si por sus extremos hidrófobos que corresponden a las cadenas hidrocarbonadas, mientras que sus extremos hidrófilos, aquellos que llevan los grupos carboxilo, ionizados negativamente por pérdida de un ion sodio o potasio, se repelen entre si. De esta manera las cadenas no polares del jabón se ocultan al agua, mientras que los grupos carboxilo, cargados negativamente, se hallan expuestos a la misma.
En la formación de una micela de jabón en agua, las moléculas de jabón (una sal de sodio o potasio de un ácido graso) se enlazan entre si por sus extremos hidrófobos que corresponden a las cadenas hidrocarbonadas, mientras que sus extremos hidrófilos, aquellos que llevan los grupos carboxilo, ionizados negativamente por pérdida de un ion sodio o potasio, se repelen entre si. De esta manera las cadenas no polares del jabón se ocultan al agua, mientras que los grupos carboxilo, cargados negativamente, se hallan expuestos a la misma.
De forma semejante, los lípidos polares en disolución acuosa diluida se dispersan formando micelas. En éstas, las cadenas hidrocarbonadas se ocultan del entorno acuoso y forman una fase hidrófoba interna, con los grupos hidrófilos expuestos en la superficie. Estas micelas pueden contener millares de moléculas de lípidos y, por tanto, su masa es muy elevada.
En disoluciones acuosas, las moléculas anfifílicas forman micelas en las que los grupos polares están en la superficie y las partes apolares quedan inmersas en el interior de la micela, en una disposición que elimina los contactos desfavorables entre el agua y las zonas hidrófobas y permite la solvatación de los grupos de las cadenas polares.
En otro tipo de medios, las moléculas anfifílicas se pueden organizar como micelas inversas.
Agua micelar, el secreto para el rostro
 Quién no ha experimentado alguna vez la dificultad de mezclar agua y aceite? Incluso, la frase “son como el agua y el aceite” se utiliza para marcar las diferencias entre dos personas y la imposibilidad de que mantengan un vínculo de cualquier índole.
Quién no ha experimentado alguna vez la dificultad de mezclar agua y aceite? Incluso, la frase “son como el agua y el aceite” se utiliza para marcar las diferencias entre dos personas y la imposibilidad de que mantengan un vínculo de cualquier índole.
Ahora bien, ¿por qué el agua y el aceite no se mezclan? El hecho es que no pueden interactuar porque tienen polaridades muy diferentes. Sin embargo, si a ese sistema agua-aceite le agregamos un tensioactivo, que es un tipo de molécula química inteligente, se puede lograr la interacción de esas dos capas completamente separadas.
Las moléculas tensioactivas tienen un extremo polar que atrae las moléculas de agua y el otro extremo no polar que atrae las de aceite. De este modo, al aproximarse, se mezclan y se forman las llamadas “micelas”.
En cosmética, este sistema de acumulación de moléculas entre líquidos coloides se utiliza sobre todo para elaborar productos de limpieza facial.
Dado que la suciedad de la piel está entremezclada con la secreción sebácea, una manera efectiva de removerla es en dos pasos: el primero, mediante la aplicación de cremas o emulsiones, y el segundo, retirando la fase grasa con abundante agua.
 El agua micelar permite remover la suciedad y retirar el residuo graso en un solo paso. El procedimiento es práctico y rápido que facilita la limpieza. De ahí su éxito, sobre todo entre las personas jóvenes que buscan simplificar sus rutinas de belleza.
El agua micelar permite remover la suciedad y retirar el residuo graso en un solo paso. El procedimiento es práctico y rápido que facilita la limpieza. De ahí su éxito, sobre todo entre las personas jóvenes que buscan simplificar sus rutinas de belleza.
Además de proveer una limpieza profunda y eliminar impurezas, el agua micelar refresca sin irritar, no deja sensación grasosa y no necesita enjuague.
¿Cómo se utiliza?
Se embebe un disco de algodón con agua micelar y se pasa por el rostro. Se repite el procedimiento hasta que el disco salga limpio. En ocasiones puede requerir dos o tres pasadas.
Es una rutina de higiene muy suave, ideal para pieles sensibles y para personas que utilizan lentes de contacto.
Luego de la limpieza se recomienda hidratar la piel y tratarla según el diagnóstico y la indicación de un profesional de la estética.